比以往任何时候都更接近于人类心脏的生物打印
虽然生物打印领域在过去几年中持续明显扩大,使得实验室中的细胞和用于打印它们的生物油墨具有更好的可持续性,但最终目标几乎总是离3D打印器官更近,这意味着它拥有巨大的潜力。美国当前医学文化的变化是,病人在等待移植的过程中遭受痛苦并经常死亡。现在,通过初创公司FluidForm和卡内基梅隆大学的合作,科学家们可能比以往任何时候都更接近于人类心脏的生物打印。
关于这一主题的研究结果最近发表在8月2日的《科学》杂志上,关于卡内基梅隆大学研究小组的工作,该研究小组由共同第一作者和FluidForm联合创始人以及其他九名成员组成。他们刚刚开发了一种高级版本的自由可逆悬浮水凝胶(FRESH)包埋技术,可以让他们3D打印胶原蛋白。有了这些新的进展,科学家们可以制造心脏部件,包括微小的血管、瓣膜和跳动的心室。
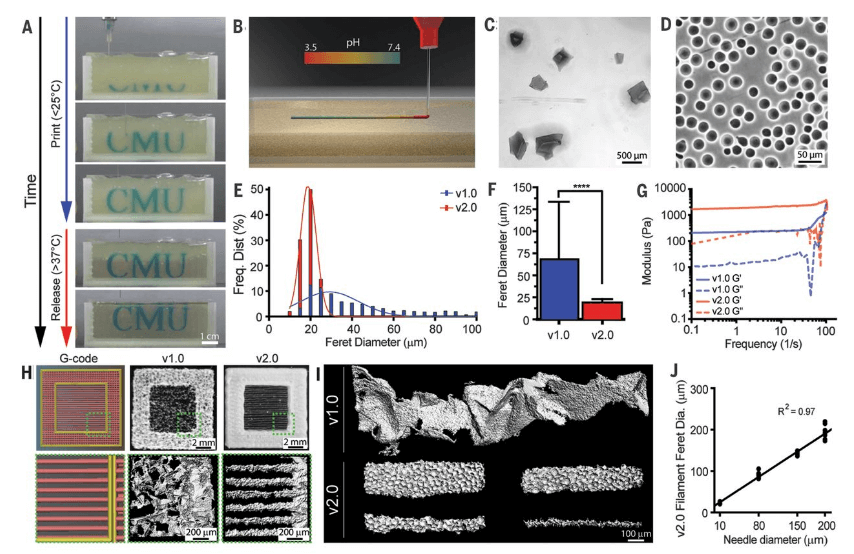
(A)使用FRESH v2.0对字母“CMU”进行3D生物打印的延时序列。(B)挤出到缓冲至pH7.4的FRESH支持浴中的酸化胶原溶液的示意图,其中快速中和引起凝胶化和胶原长丝的形成。(C和D)(C)FRESH v1.0和(D)v2.0的支持浴中明胶微粒的代表性图像,显示尺寸和多分散性的降低。(E)FRESH v1.0(蓝色)和v2.0(红色)中明胶微粒的Feret直径分布的直方图。(F)FRESH v1.0和v2.0的明胶微粒的平均Feret直径[N> 1200,数据是平均值±SD,**** P <0.0001(Student t检验)]。(G)FRESH v1.0和v2.0载体浴的储存(G')和损失(G“)模量,显示屈服应力流体行为。(H)一个“窗框”打印结构,中间是单丝,比较G代码(左),FRESH v1.0(中)和FRESH v2.0(右)。(I)使用FRESH v1.0(下图)使用FRESH v1.0(上图)显示最小直径(~250μm)的可变性,与使用FRESH v2.0(下图)直径20至200μm的相对光滑的长丝相比。(J)胶原长丝Feret直径作为挤压针内径的函数为FRESH v2.0,呈线性关系。
这项重要工作的专利属于FluidForm,总部位于匹兹堡和波士顿。
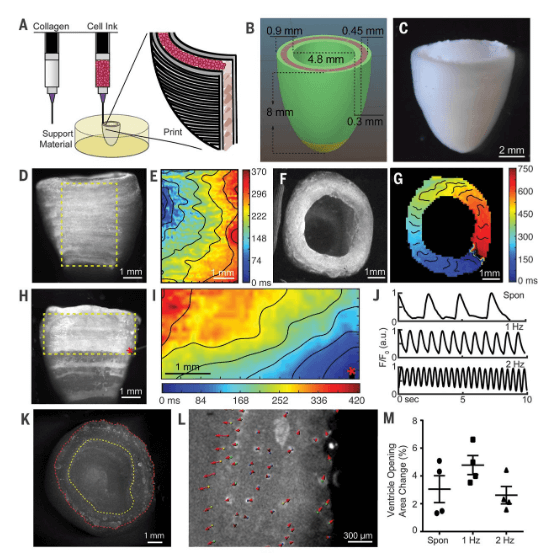
根据核磁共振成像数据,FRESH生物打印心脏由小心室组成,其上印有人体心肌细胞,显示如下:
同步收缩
定向作用电位传播
在收缩高峰期,壁厚增厚达14%
“我们发现FRESH 3D生物打印的心脏能够准确地再现患者特异性的解剖结构,这是由微型计算机断层扫描确定的。用人心肌细胞打印的心室显示同步收缩,定向动作电位传播,以及在收缩高峰期间壁厚增厚达14%。”研究人员在他们的论文中说,”3D生物打印胶原蛋白以重建人类心脏的组成部分。”
然而,随着科学家们努力产生3D打印更大组织所需的数十亿个细胞,其他的障碍仍然存在。
研究人员在他们的论文中说:“虽然一个功能齐全的器官的三维生物打印还没有实现,但我们现在有能力构建结构,开始重新描述原生组织的结构、机械和生物特性。”
虽然以前的科学家已经预测在不久的将来会对器官进行生物打印,但事实证明,它显然要比预期的要困难得多。里程碑继续被超越,但挑战继续爆发。主要是通过与适当的技术协调保持细胞活力 - 意义材料,软件和硬件继续成为重点。使用FRESH,临时支持凝胶用于3D打印胶原蛋白支架,由驱动胶原蛋白自组装的快速pH变化驱动。然而,不仅对3D打印心脏有希望,而且未来还有一系列不同的组织和器官。
FluidForm首席执行官Mike Graffeo表示:“FluidForm对在Feinberg实验室进行的研究感到非常自豪。卡内基梅隆大学开发的新技术使生物打印研究人员能够实现前所未有的结构、分辨率和保真度,这将使该领域的量子跃进。我们很高兴能为世界各地的研究人员提供这项技术。”

(A)FRESH打印的胶原管构造。(B)将C2C12细胞和胶原凝胶混合物浇铸在胶原管周围并静置培养5天。(C)来自(B)的组织的横截面染色用于活(绿色)和死(红色)细胞。(D)将C2C12细胞和胶原凝胶混合物浇铸在胶原管周围并灌注5天。(E)来自(D)的组织的横截面针对活细胞和死细胞染色。(F)作为来自静态和灌注胶原管构建体的组织顶部表面的深度的函数的细胞存活率百分比[N = 3,数据是平均值±SD,* P <0.05(双向ANOVA,其次是Bonferroni倍数)- 比较后测试)]。(G)多光子成像显示在去除明胶微粒支持浴后FRESH打印的胶原构建体中的微观孔隙率。(H和I)皮下植入后7天,没有VEGF的胶原蛋白构建体(H)和FRESH-打印(I)。(J和K)Masson三色染色以在皮下植入7天后观察铸型(J)和FRESH-打印(K)胶原盘中的细胞(红色)和胶原(蓝色)。(L)植入后的细胞密度作为铸造和FRESH打印的胶原盘的深度的函数。(M和N)胶原构建体在皮下植入10天后用VEGF(100ng / ml)铸造(M)和FRESH-打印(N)。在皮下植入10天后,(O和P)CD31染色(棕色)和掺有VEGF(100ng / ml)的铸造(O)和FRESH-打印的(P)胶原盘的细胞(蓝色)。(Q)通过凝集素尾静脉注射(红色)标记的FRESH印迹胶原盘中的血管(直径8至50μm)的血管浸润。(R)多光子图像70μm进入FRESH打印的构建体,显示微血管腔内的红细胞。
FluidForm推出其首款产品LifeSupport™生物打印支持凝胶,将FRESH技术商业化,并为各地的科学家和研究人员提供3D打印胶原、细胞和生物材料的机会。
(A)FRESH打印的胶原管构造。(B)将C2C12细胞和胶原凝胶混合物浇铸在胶原管周围,并静置培养5天。(C)来自(B)的组织的横截面染色用于活(绿色)和死(红色)细胞。(D)将C2C12细胞和胶原凝胶混合物浇铸在胶原管周围并灌注5天。(E)来自(D)的组织的横截面针对活细胞和死细胞染色。(F)作为来自静态和灌注胶原管构建体的组织顶部表面的深度的函数的细胞存活率百分比[N = 3,数据均为平均值±标准差,* P <0.05(双向方差分析,随后进行Bonferroni多重比较测试)。(G)多光子成像显示在去除明胶微粒支持浴后FRESH打印的胶原构建体中的微观孔隙率。(H和I)皮下植入后7天,胶原构建物铸型(H)和FRESH打印型(I)。在铸型(J)和FRESH打印的(K)胶原盘中显示细胞(红色)和胶原(蓝色)。(L)植入后的细胞密度作为铸造和FRESH打印的胶原盘的深度的函数。(M和N)胶原构建体在皮下植入10天后用血管内皮生长因子(100ng / ml)构建模型(M)和FRESH-打印型(N)。在皮下植入10天后,(O和P)CD31染色(棕色)和掺有血管内皮生长因子(100ng / ml)的构建型(O)和FRESH-打印的(P)胶原盘的细胞(蓝色)。(Q)通过凝集素尾静脉注射(红色)标记的FRESH印迹胶原盘中的血管(直径8至50μm)的血管浸润。 (R)多光子图像70μm进入FRESH打印的构建体,显示微血管腔内的红细胞。













